さて、ここではタンパク質を構成するアミノ酸について解説します。
タンパク質を構成するアミノ酸とは
さて、タンパク質を構成するのはアミノ酸であり、アミノ酸とは、アミノ基「-NH2」とカルボキシ基「-COOH」を持つ有機化合物のことです。
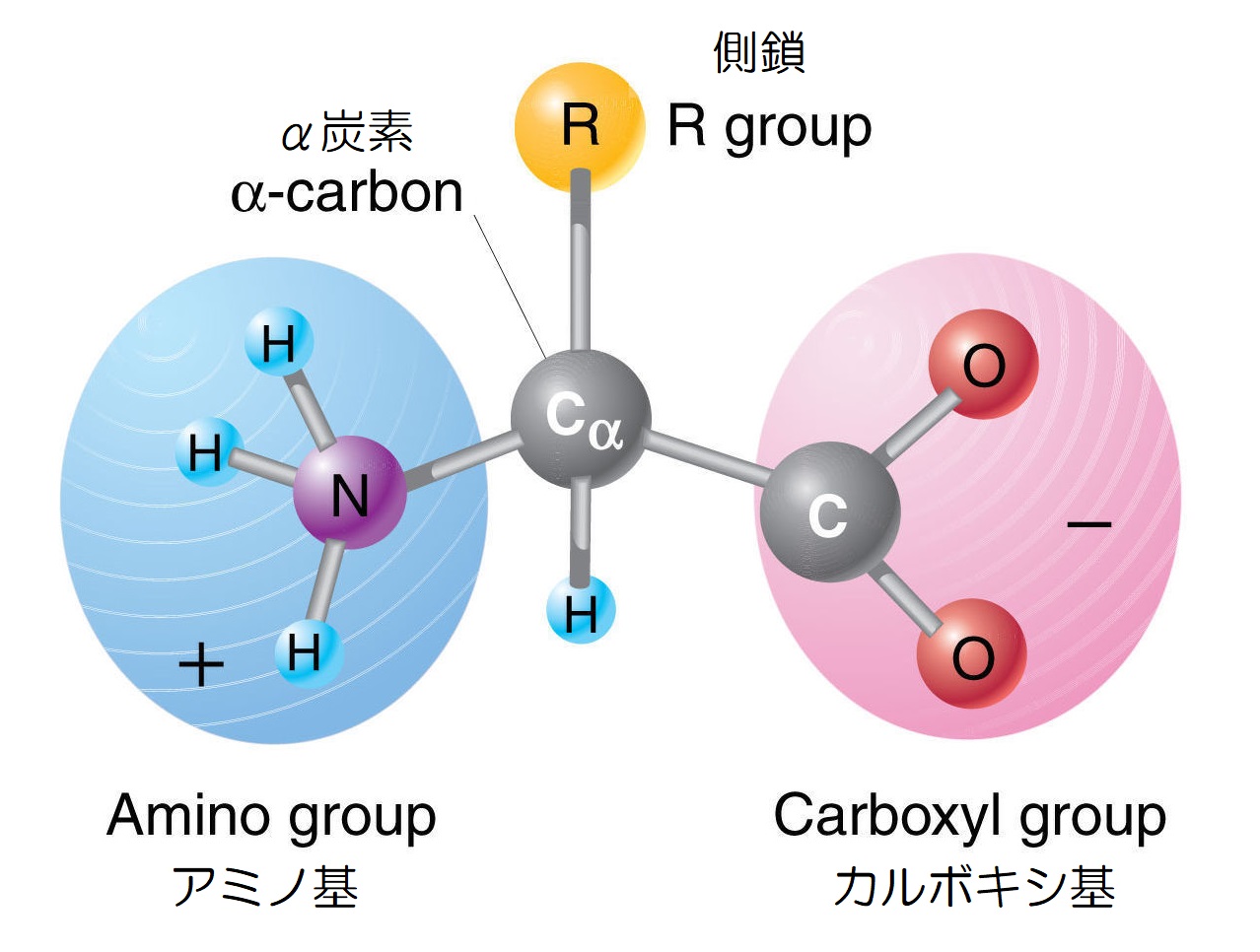 ▲アミノ酸の構造(引用:Ezam a2z)
▲アミノ酸の構造(引用:Ezam a2z)
アミノ基は塩基性、カルボキシ基は酸性を示すため、アミノ酸は両性化合物であり、水溶液中ではカルボキシ基の水素イオンがアミノ基に移り、分子内塩を構成します。
そして、アミノ基とカルボキシ基が同じ炭素原子に付くと、その炭素原子を「α炭素」、そのアミノ酸を「αアミノ酸」と呼び、人体を構成する20種のアミノ酸はすべてαアミノ酸です。
L型アミノ酸とは
炭素原子には4つの結合の手がありますので、アミノ基とカルボキシ基以外の手には、「水素原子H」と、他の原子団である「側鎖」が付いた構造を取ります。
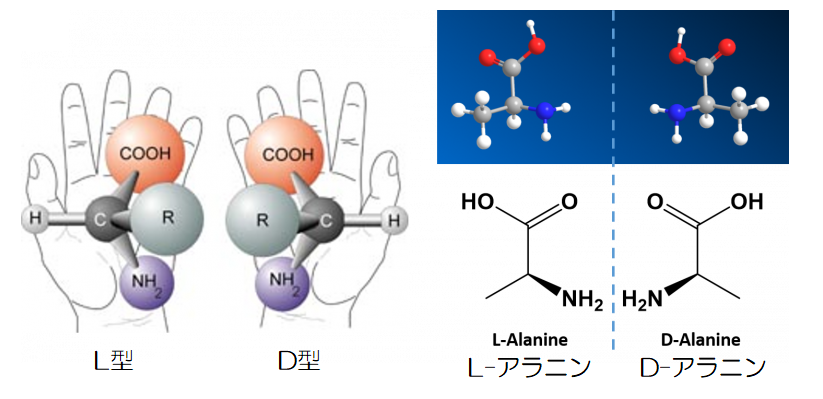 ▲L型アミノ酸とD型アミノ酸(引用:Slide ToDoc)
▲L型アミノ酸とD型アミノ酸(引用:Slide ToDoc)
側鎖「R」はアミノ酸の種類を分ける構造であり、この違いにより、親水性や疎水性、高次構造の際の分子間力などの性質を生み出し、多彩なタンパク質を作り出します。
また、アミノ酸は立体構造を取るため、同じ炭素原子に全て異なる原子団が結合していると、構成する原子は同じなのに、左手と右手のように重なり合わない「鏡像異性体」が存在することになります。
鏡像異性体にはL型とD型があり、L型は水素を手前にした場合、右回りに「カルボキシ基→側鎖→アミノ基」となり、人体を構成するアミノ酸はすべてそのL型です。
アミノ酸の種類
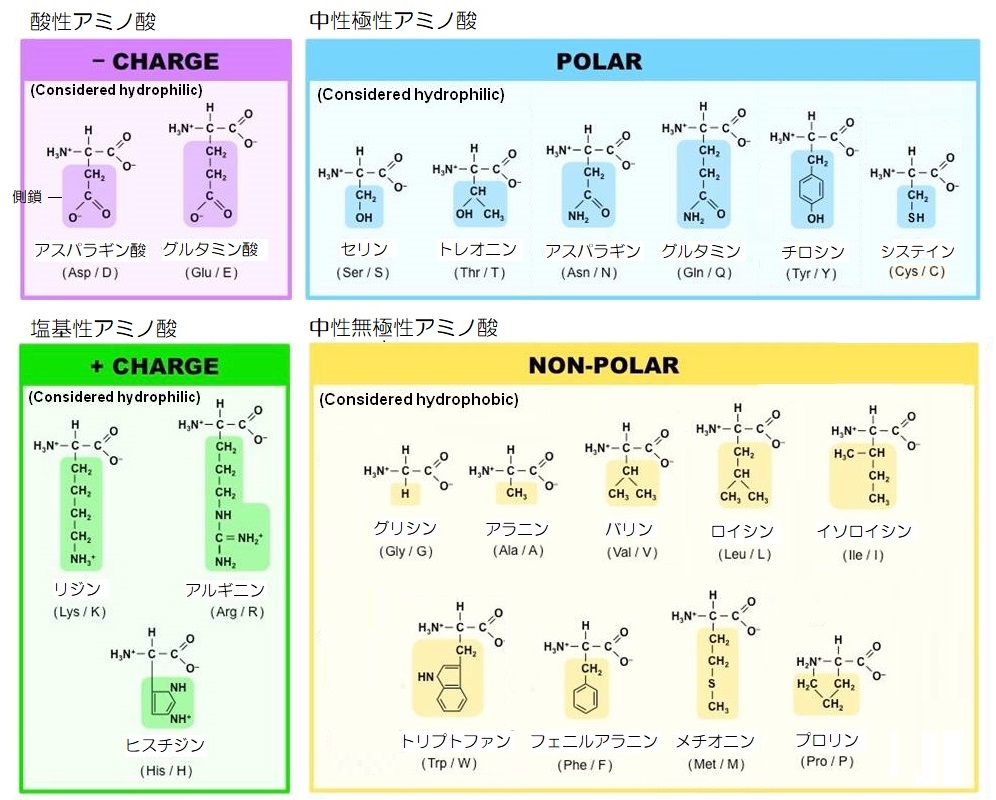
アミノ酸は、天然には約500種類ありますが、人体を構成するアミノ酸は20種類のみで、これを標準アミノ酸と呼び、側鎖Rの構造により次のように分類されます。
アミノ酸には側鎖の構造により、酸性アミノ酸、塩基性アミノ酸、中性極性アミノ酸、中性無極性アミノ酸に分類され、前者3つが親水性、最後が疎水性です。
アスパラギン酸とグルタミン酸は、側鎖にカルボキシ基を持ち、水溶液中で水素イオンが電離しますので酸性アミノ酸であり、親水性を示します。
アルギニン、ヒスチジン、リジン(リシン)は、側鎖にアミノ基を持ち、水溶液中で水素イオンを得るため塩基性アミノ酸であり、これも親水性です。
他のアミノ酸は全て中性ですが、セリン、トレオニン、アスパラギン、グルタミン、チロシン、システインは側鎖の極性が強いため、中性極性アミノ酸で親水性です。
一方、グリシン、アラニン、バリン、ロイシン、イソロイシン、フェニルアラニン、トリプトファン、メチオニン、プロリンは側鎖の極性が弱く、中性無極性アミノ酸で疎水性です。
ただ、極性の分類は尺度により異なり、システインが疎水性に分類されたり、グリシンが親水性に分類されたりすることもあります。
極性とは
アミノ酸の分類にある、「極性」「無極性」とは、分子内に電気的な偏りがあるかないかの違いで、その偏りにより親水性か疎水性かの性質に分かれます。
異なる原子が結合した分子は、共有結合している部分で電子を引き付ける力(電気陰性度)が異なり、電気陰性度の高い原子の方に電子が引き寄せられます。
すると、同じ分子内で電気的な偏りが生じる場合があり、電気的な偏りがある分子を「極性分子」、偏りがない分子を「無極性分子」と呼びます。
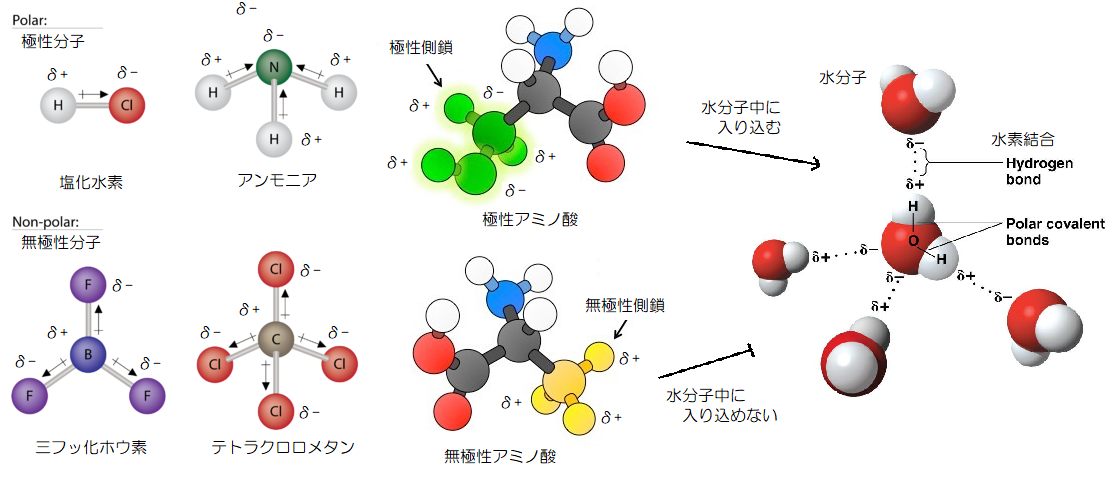 ▲極性分子と無極性分子(引用:Quora、Wikipedia)
▲極性分子と無極性分子(引用:Quora、Wikipedia)
水分子は、酸素原子が電子を引き付ける力が強く、酸素原子がマイナス、水素原子がプラスの電荷に偏り、水分子どうしで電気的に引き合う水素結合で結ばれています。
ここに、同じく電気的な偏りある極性分子が入り込むと、水分子の水素結合間に取り込まれるため、水に溶けやすくなります。
逆に電気的な偏りがない無極性分子では、水素結合間に入り込みにくく、水分子内に取り込まれないため、水に溶けにくい性質を持ちます。
アミノ酸の側鎖部分に、極性があれば水に溶けやすい「親水性アミノ酸」に分類され、側鎖が無極性の場合は、水に溶けにくい「疎水性アミノ酸」になります。
ペプチド結合とは
さて、アミノ酸のカルボキシ基「-COOH」は、別のアミノ酸のアミノ基「-NH2」と、水分子「H2O」が取れて結合し、これを「アミド結合(ペプチド結合)」と呼びます。
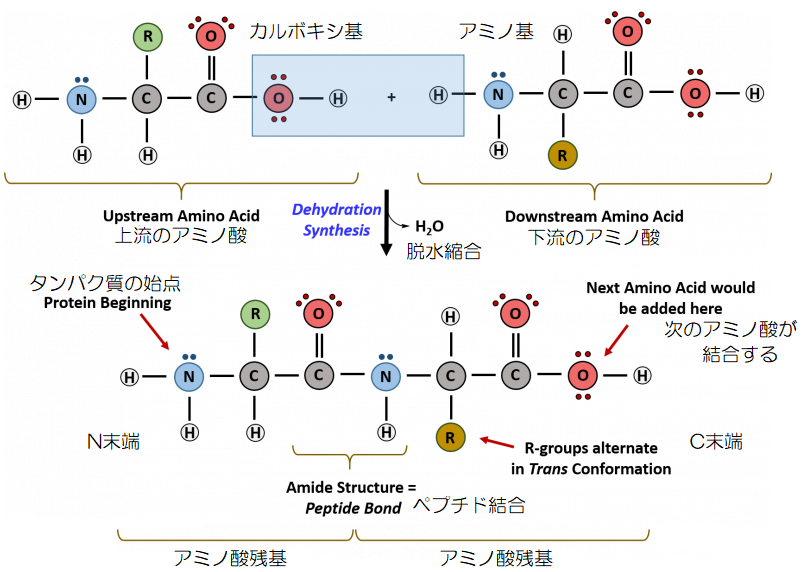 ▲アミノ酸のペプチド結合
▲アミノ酸のペプチド結合
そして、多数のアミノ酸が次々につながったものを「ポリペプチド」と呼び、水分子が取れて残ったアミノ酸の部分のことを「アミノ酸残基」と呼びます。
両端のアミノ基とカルボキシ基は結合せずに残っていますので、残ったアミノ基側を「N末端」、カルボキシ基側を「C末端」と呼び、N末端がタンパク質の始まりです。
多くのタンパク質はこのアミノ酸が100~400個ほど繋がって構成され、毛髪も400個ほどのアミノ酸が繋がり、ケラチンモノマーという基本単位を作ります。
このアミノ酸が多数連結した、ポリペプチド鎖の構造を「タンパク質の一次構造」と呼びます。
タンパク質の二次構造「αヘリックス」
さて、アミノ酸がペプチド結合すると、繋がった部分にカルボニル基「-C=O」とイミノ基「-N-H」の構造がたくさん残ります。
酸素原子Oと窒素原子Nは電気陰性度(電子を引きつける力)が高いため、「-C=O」の酸素原子Oがマイナス(δー)に、「-N-H」の水素原子Hがプラス(δ+)に帯電します。
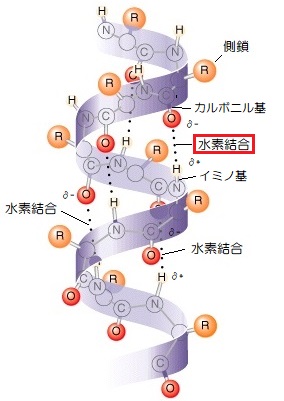 ▲タンパク質のαヘリックス構造と水素結合(引用:Griffiths et al.)
▲タンパク質のαヘリックス構造と水素結合(引用:Griffiths et al.)
ペプチド鎖が長くなってくると、上図のように「-C=O(δ-)…(δ+)H-N-」と、電気的に引き合う場所が生まれ、これを水素原子を介した結合のため「水素結合」と呼びます。
この水素結合がアミノ酸4残基分離れた場所で繰り返すと、長いポリペプチド鎖は右巻き螺旋状の構造になり、これをαヘリックス構造と呼び、ヘリックスとは螺旋という意味です。
水素結合は、静電気的な引力なので電子を共有する共有結合ほどは強くありませんが、多数の結合が規則正しく並んでいるので非常に安定しています。
そして、螺旋構造の内側は、隙間がないくらい密に詰まっていて、側鎖Rの部分はすべて螺旋の外側を向いているという特徴があります。
このαヘリックスの構造を「タンパク質の二次構造」と呼びます。
タンパク質の二次構造「βシート、βターン」
そして、タンパク質の二次構造には、αヘリックス以外にも、βシートやβターン構造と呼ばれるものもあります。
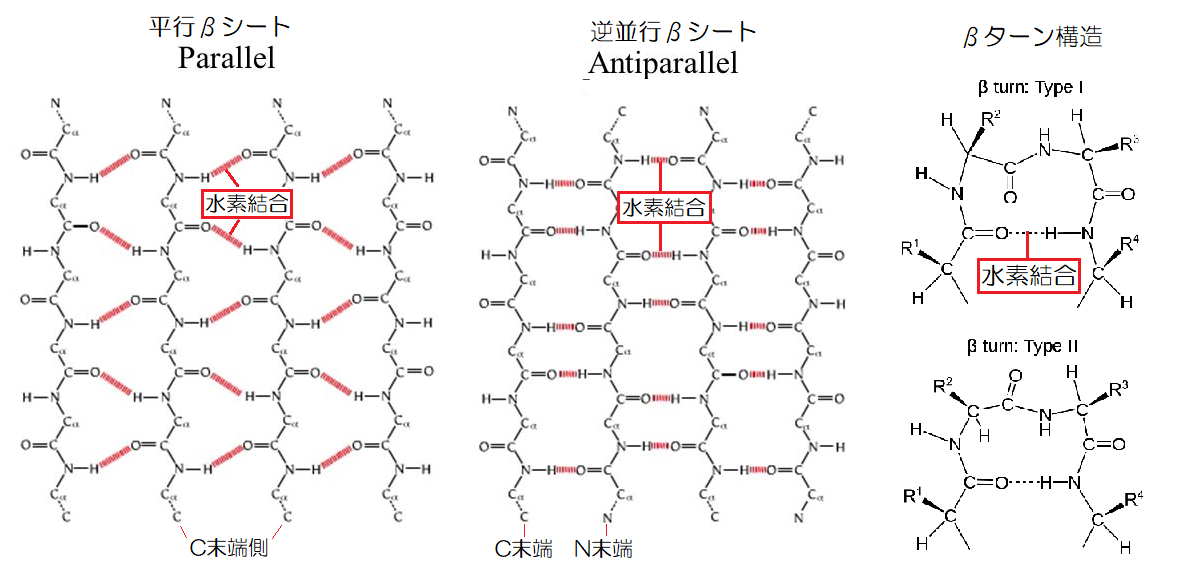 ▲タンパク質のβシートとβターン構造(引用:SlidePlayer)
▲タンパク質のβシートとβターン構造(引用:SlidePlayer)
βシートは、ポリペプチド鎖が平面状で、カルボニル基(ーC=O)とイミノ基(-N-H)の部分で電気的に引き合う水素結合を形成しています。
ポリペプチド鎖はN末端とC末端の方向性があり、N末端が同じ側を向いた「平行βシート」と、逆を向いた「逆並行βシート」があります。
また、βターンは4つのアミノ酸で180度折れ曲がり構造を作るときに現れ、1番目と4番目のアミノ酸の側鎖のカルボニル基とイミノ基で水素結合を結んでいます。
このように、タンパク質の二次構造は、αヘリックス、βシート、βターンなど、多数の水素結合の作用により構成されています。
そして、この二次構造には、αヘリックスが多いタンパク質と、βシートが多いタンパク質、αヘリックスとβシートの両方で成り立っているタンパク質などがあります。