ここでは、縮毛矯正をかけたことがある方なら馴染み深い、タンパク質の三次構造をなす側鎖間の結合の種類について解説します。
タンパク質の三次構造
さて、タンパク質はアミノ酸がペプチド結合をして一次構造を形成し、その後、カルボニル基とイミノ基の部分で水素結合を繰り返すことにより二次構造を形成しました。
しかし、タンパク質はここで完成する訳ではありません。
螺旋状やシート状になった二次構造のタンパク質は、その後、残された側鎖Rの部分どうしでさまざまな作用が働くことで、さらに複雑な立体構造を作り出します。
 ▲アミノ酸残基の側鎖間での結合の種類(引用:Sam Adam-Day)
▲アミノ酸残基の側鎖間での結合の種類(引用:Sam Adam-Day)
システインの側鎖どうしの「ジスルフィド結合」、リジンと酸性アミノ酸の側鎖どうしによる「イソペプチド結合」は共に共有結合であり、非常に強固な結合になります。
また、側鎖のヒドロキシ基とカルボニル基による「水素結合」、酸性アミノ酸と塩基性アミノ酸の側鎖どうしの「イオン結合」は共に静電気的な引力であり、若干弱い結合です。
そして、ベンゼン環や炭化水素基などの無極性側鎖どうしでの「疎水性相互作用」という作用もあり、これは最も弱い結合になります。
これらのさまざまな結合により、タンパク質は複雑な立体構造をなし、これをタンパク質の三次構造と呼びます。
ジスルフィド結合
ジスルフィド結合は、システインの側鎖であるチオール基(SH基)どうしの水素が取れることで酸化され、シスチンになる共有結合です。
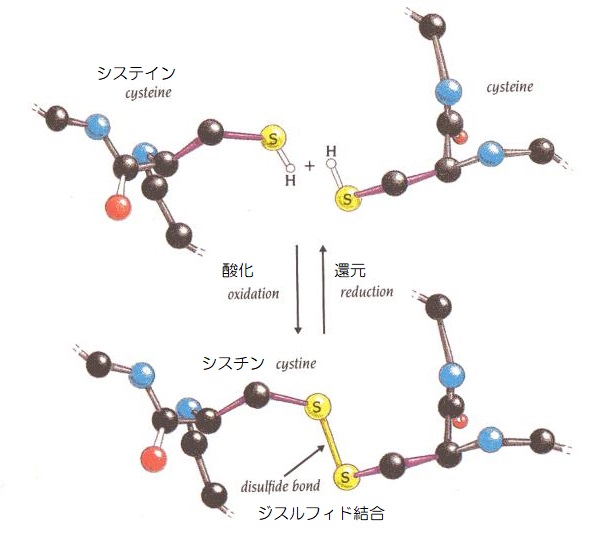 ▲ジスルフィド結合
▲ジスルフィド結合
タンパク質の高次構造の中では、数少ない共有結合ですので、その結合力は非常に強力で、タンパク質の立体構造の安定性を保ちます。
そのため、より強度が必要な皮膚や毛髪、爪などを構成するケラチンにはシステインが非常に多く含まれ、内部に多数のジスルフィド結合を持っています。
縮毛矯正やパーマなどでは、「S-S結合」「シスチン結合」などと呼ばれ、頻繁に出てくるため、くせ毛の方は馴染み深いと思います。
このように、チオール基を持つものは「チオール」と呼ばれ、硫黄を含むため悪臭を放つものが多いのが特徴です。
そのため、パーマなどの還元剤でジスルフィド結合を切断するとチオールが生じて臭いを放つのです。
イソペプチド結合
イソペプチド結合とは、タンパク質の一次構造の際のペプチド結合ではなく、三次構造において、側鎖どうしでのペプチド結合のことを言います。
 ▲イソペプチド結合(引用:Registry of Standard Biological Parts)
▲イソペプチド結合(引用:Registry of Standard Biological Parts)
アルパラギン酸やグルタミン酸などの酸性アミノ酸は側鎖にカルボキシ基を持っていて、塩基性アミノ酸であるリジンは、側鎖にアミノ基を持っています。
このカルボキシ基とアミノ基はトランスグルタミナーゼの酵素により、一次構造と同じように脱水縮合してペプチド結合を形成し、これを特にイソペプチド結合と呼びます。
これも、ジスルフィド結合と同じく強固な共有結合のため、タンパク質の立体構造を安定化させる上で、非常に重要な役割を果たします。
毛髪では、キューティクルの最外層であるエピキューティクルやメデュラに存在し、毛髪を最外層から、また最内層から強度を持たせることにより、化学的に安定させています。
イオン結合
イオン結合は、アミノ酸の側鎖がプラスの電荷を持つものと、マイナスの電荷を持つものとの間による静電気的な力による化学結合です。
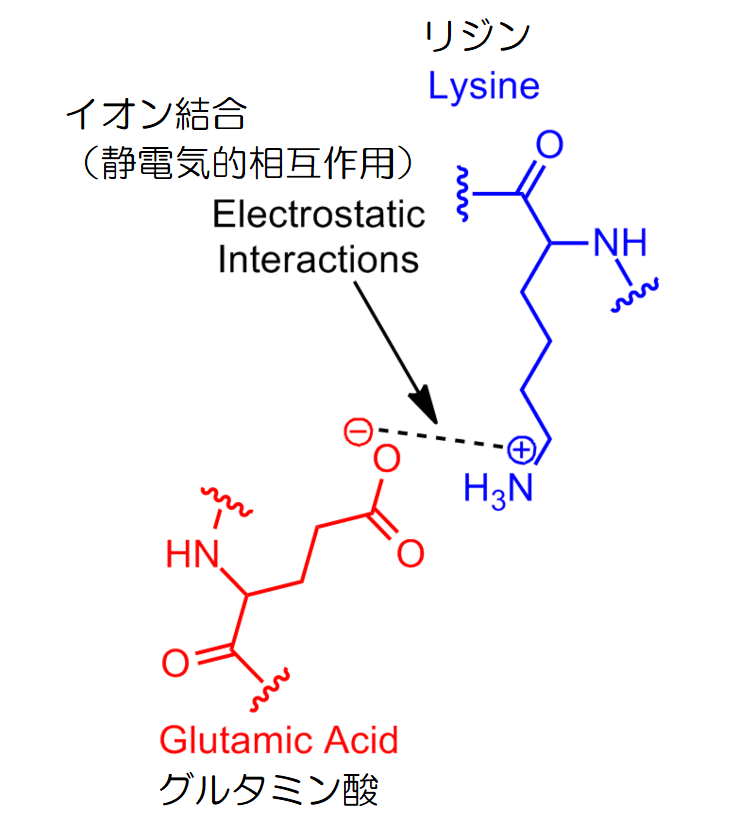 ▲リジンとグルタミン酸によるイオン結合(引用:wikipedia)
▲リジンとグルタミン酸によるイオン結合(引用:wikipedia)
イオン結合は、「塩結合」「塩橋」「静電気的相互作用」とも呼ばれ、電荷を帯びているため、その結合力は水素結合より強いですが、共有結合よりは劣ります。
アミノ酸は中性の水溶液中ではイオンの状態で存在し、酸性アミノ酸のアスパラギン酸やグルタミン酸はカルボキシ基の水素イオンが電離し「COO-」とマイナスの電荷を帯びます。
一方、塩基性アミノ酸のリジンやアルギニンは、アミノ基に水素イオンが結合し、「NH3+」とプラスの電荷を帯び、これがお互いに静電気的に引き合うのです。
水素原子を介した部分は水素結合ですが、
水素結合
タンパク質の二次構造で、αヘリックスやβシートなどを形成する作用が水素結合ですが、三次構造においても、側鎖どうしで水素結合を構成するものがあります。
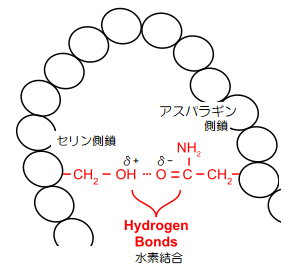 ▲セリンとアスパラギンによる水素結合
▲セリンとアスパラギンによる水素結合
セリンやチロシンなど、側鎖にヒドロキシ基(OH基)を持つものは、酸素側に電子が偏るため、水素原子がプラスの荷電を帯びます。
一方、アスパラギン酸やグルタミン酸、アスパラギンなどのアミノ酸は、側鎖にカルボニル基(-C=O)を持ち、酸素原子がマイナスの電荷を帯びます。
すると、ヒドロキシ基の水素(H)とカルボキシ基の酸素(O)が静電気的に引き合い、水素原子を介した水素結合が結ばれます。
疎水性相互作用
疎水性相互作用とは、水分子などの極性がある溶液中では、無極性分子(疎水性分子)が水分子に弾かれて、集まり合う性質のことです。
 ▲無極性分子どうしは水分子中では集まる性質がある(引用:hotcore.info)
▲無極性分子どうしは水分子中では集まる性質がある(引用:hotcore.info)
水分子どうしは互いに水素結合を結んで繋がっていますが、そこに無極性分子が入ると、水分子の水素結合に弾かれ、無極性分子どうしが集まろうとする力が働きます。
この作用のことを「疎水性相互作用」と呼びますが、無極性分子どうしに結合が生じている訳でもないため、その作用は弱いものとなっています。
しかし、タンパク質の三次構造を作る上では、周りの水分子を嫌って、側鎖の疎水基どうしが内側に畳まれる構造をとるため、非常に重要な作用になります。
タンパク質では、側鎖のベンゼン環や炭化水素基が無極性分子のため、フェニルアラニンやバリン、ロイシンなどの側鎖どうしが疎水性相互作用を形成します。
タンパク質の四次構造
さて、一本のポリペプチド鎖からなるタンパク質は三次構造で完成します。
しかし、その三次構造のポリペプチド鎖が集って、互いに非共有結合などにより結びつくことでさらに大きな単位になり、ようやく機能を持つものも多くあります。
これをタンパク質の四次構造と呼びます。
この四次構造では、一つのポリペプチド鎖をサブユニットと呼び、一つのサブユニットで機能するタンパク質を単量体、2つ集まったものを二量体、3つでは三量体と呼びます。
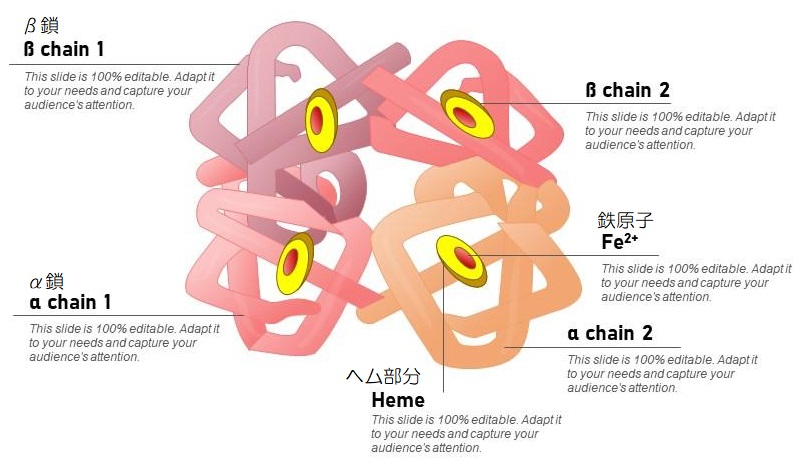 ▲ヘモグロビンの構造(引用:Slide Team)
▲ヘモグロビンの構造(引用:Slide Team)
赤血球で酸素を運ぶタンパク質として有名なヘモグロビンは、αグロビンとβグロビンというタンパク質が2つずつ、合計4つ組み合わさった四量体のタンパク質になります。
グロビンには二価の鉄原子を持ったヘムという赤い色素が含まれていて、これに酸素分子が結合することにより、ヘモグロビンは一度に4つの酸素分子を運ぶことができるのです。